Pressione Enter para pesquisar ou ESC para sair
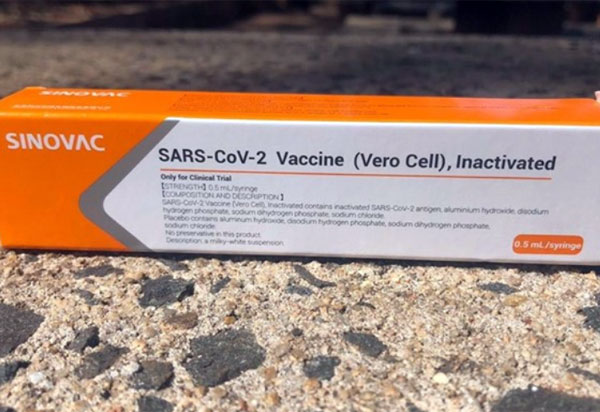
O governo brasileiro vai comprar 46 milhões de doses da Coronavac, vacina do Instituto Butantan produzida em parceria com a empresa chinesa Sinovac, conforme foi anunciado em reunião com governadores nesta terça-feira (20). De acordo com informações do ministro da Saúde, Eduardo Pazuello, as doses serão distribuídas a todo o Brasil por meio do Programa Nacional de Imunizações (PNI), que há décadas já garante o sucesso das campanhas nacionais de vacinação. Antes do anúncio desta terça-feira, a previsão do ministério era ter 140 milhões de doses no primeiro semestre de 2021.
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou a Jansen-Cilag, unidade farmacêutica da Johnson & Johnson, a realizar testes clínicos no Brasil para o desenvolvimento de vacina contra a covid-19. O estudo global prevê a inclusão de até 60 mil voluntários, sendo 7 mil no Brasil, distribuídos nos estados de São Paulo, Rio Grande do Sul, Rio de Janeiro, Paraná, Minas Gerais, Bahia e Rio Grande do Norte. Em nota divulgada hoje (18), a Anvisa informou que os dados que embasaram a autorização incluíram estudos não clínicos com a vacina e dados não clínicos e clínicos acumulados de outras vacinas que utilizam a mesma modelagem. Os estudos da Jansen-Cilag foram iniciados em julho nos EUA e na Bélgica. De acordo com a agência, o ensaio clínico será conduzido em etapas e cada etapa só será iniciada se os resultados que estiverem disponíveis no momento forem satisfatórios. Este é o quarto estudo de vacina contra o novo coronavírus autorizado pela Anvisa no Brasil. No dia 2 de junho, a agência autorizou o ensaio clínico da vacina desenvolvida pela empresa AstraZeneca e pela Universidade de Oxford, do Reino Unido; no dia 3 de julho, o da vacina desenvolvida pela Sinovac Biotech, da China, em parceria com o Instituto Butantan; e no dia 21 de julho, o das vacinas desenvolvidas pela BioNTech, da Alemanha, e Wyeth/Pfizer, dos Estados Unidos. A potencial vacina da Jansen-Cilag, denominada Ad26.COV2.S, é composta de um vetor recombinante, não replicante, de adenovírus tipo 26 (Ad26), construído para codificar a proteína S (Spike) do vírus Sars-CoV-2 (o novo coronavírus).
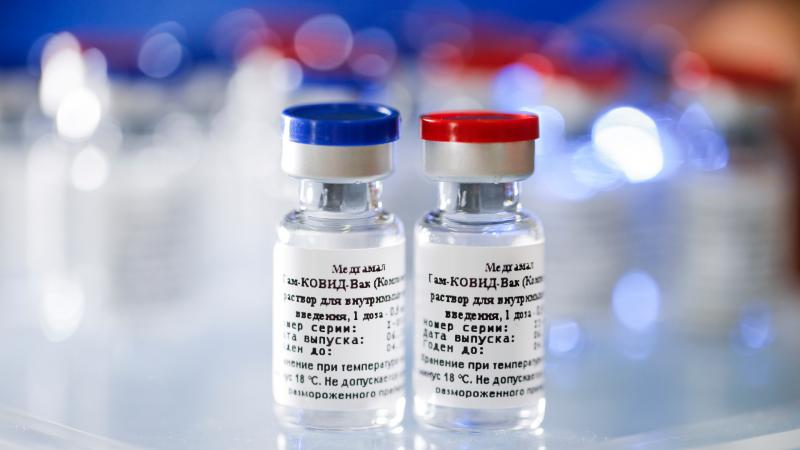
Por meio de comunicado, a embaixada da Rússia no Brasil afirmou que negocia com o governo da Bahia para o estabelecimento de uma parceria para testes e produção da Sputnik V, primeira vacina contra o novo coronavírus registrada no mundo. “Em 30 de julho o Embaixador da Rússia teve uma reunião virtual com o governador da Bahia Rui Costa e o Secretário da Saúde do estado Fábio Vilas-Boas”. De acordo com informações da CNN, a embaixada disse ainda que o Fundo de Investimentos Diretos da Rússia (RDIF), que financia o desenvolvimento da Sputnik V, também negocia diretamente com outras instituições de pesquisa, empresas e produtores brasileiros para estabelecer parcerias na distribuição de testes e medicamentos, assim como para o desenvolvimento e produção da vacina contra o novo coronavírus. “Esperamos que daqui a pouco vejamos os frutos concretos desta cooperação”, disse a embaixada russa.

Na manhã desta sexta-feira (7), o governador Rui Costa, juntamente com o secretário estadual de Saúde, Fábio Vilas-Boas, e a secretária de Ciência e Tecnologia, Adélia Pinheiro, participou de uma teleconferência com um grupo composto por duas empresas chinesas que estão desenvolvendo duas linhas de vacinas contra a Covid-19.
"Nós fizemos o contato com eles para que o Nordeste, e obviamente a Bahia, participassem dessa pesquisa. Eles concordaram e ainda hoje enviarão os documentos para que a gente assine um protocolo conjuntamente já na próxima semana. A partir daí, pediremos autorização à Comissão Nacional de Ética e Pesquisa, do Conselho Nacional de Saúde, e também da Anvisa, para fazermos os testes dessa vacina", explicou o governador. Ainda segundo Rui, se os testes forem aprovados, os lotes da vacina devem ser enviados em 30 dias. "Seriam em torno de 4 mil pacientes testados por aqui. Essa vacina já foi aplicada em 100 mil chineses e também em outros países". O governador também lembrou que a Bahia já participa de um teste de uma empresa americana. "Além disso, vamos assinar um documento com uma empresa russa para fazer um teste com a vacina desenvolvida por eles. Com isso, estamos buscando aproximar o intercâmbio científico de pesquisa e de saúde e ao mesmo tempo nos colocando na frente para termos acesso às primeiras vacinas oferecidas, para imunizar a nossa população".
Durante audiência ao Congresso americano, nesta terça-feira (21), representantes de companhias farmacêuticas e de biotecnologia que trabalham para desenvolver vacinas para a Covid-19 disseram que estão encaminhadas para ter uma possível vacina para o fim deste ano ou no começo do próximo. Uma delas, inclusive, espera ter uma pronta a partir de setembro. De acordo com informações da CNN Brasil, Mene Pangalos, vice-presidente executivo de pesquisa e desenvolvimento de biofarmacêuticos da Astrazeneca, disse à Comissão de Energia e Comércio da Câmara dos Deputados que a vacina da empresa poderá ser disponibilizada "em qualquer momento a partir de setembro", se tudo correr bem nos testes clínicos. Os resultados preliminares do estudo das fases 1 e 2 da vacina contra o novo coronavírus desenvolvida pela Universidade de Oxford em conjunto com a Astrazeneca sugerem que ela é segura e induz resposta imune. A vacina provocou produção de anticorpos em 28 dias e produção de células T dentro de 14 dias, segundo pesquisa publicada na revista médica The Lancet nesta segunda (20). A candidata ainda está em fase de testes clínicos.
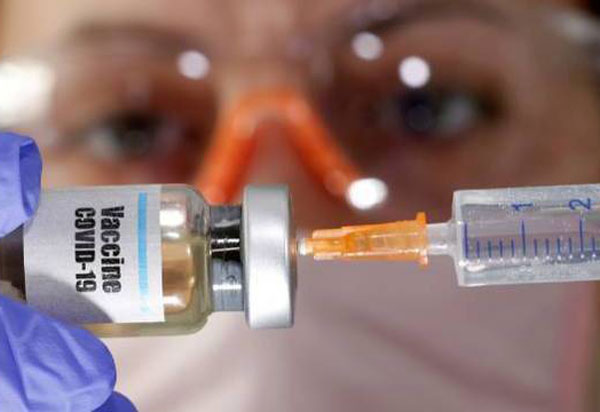
Cientistas da Universidade de Oxford, no Reino Unido, anunciaram nesta segunda-feira que, de acordo com resultados preliminares, a vacina da universidade para a Covid-19 é segura e induziu resposta imune. Os resultados, que já eram aguardados pelos pesquisadores, se referem às duas primeiras fases de testes da imunização. A terceira Fase está ocorrendo em alguns países, entre eles o Brasil. O efeito deve ser reforçado após uma segunda dose da vacina, segundo os cientistas. As fases 1 e 2 dos testes, que foram conduzidas simultaneamente no Reino Unido, tiveram 1.077 voluntários. Os ensaios mostraram que a vacina foi capaz de induzir a resposta imune tanto por anticorpos como por células T até 56 dias depois da administração da dose.

Doses da vacina do laboratório chinês Sinovac Biotech podem começar a ser testados nesta segunda-feira (20), em São Paulo. Os testes com os voluntários vai ser realizada em parceria com o Instituto Butantan. As doses da vacina chegaram ao Brasil, no aeroporto de Cumbica, em Guarulhos, na madrugada de hoje. Ao todo, nove mil voluntários vão receber a vacina contra o coronavírus. O cadastro começou a ser realizado, na última quarta-feira (15). As inscrições continuam abertas e a prioridade é testar profissionais da área da saúde.
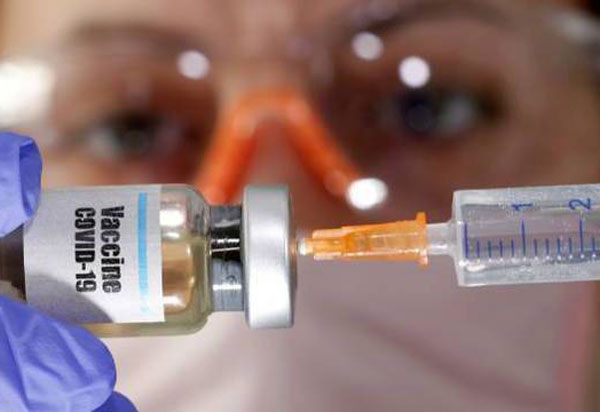
Conforme divulgado nesta segunda-feira (13) pela agência de notícias RIA, um instituto russo que está desenvolvendo uma das possíveis vacinas contra o novo coronavírus espera começar a fase final de testes em uma pequena parte do público em meados de agosto. De acordo com informações da CNN, os primeiros resultados do primeiro teste humano em pequena escala da vacina desenvolvido pelo Instituto Gamaleya em Moscou mostraram que ela é segura para uso, de acordo com um relatório. Globalmente, das 19 vacinas experimentais COVID-19 em testes em humanos, apenas duas estão em testes finais da fase 3: uma da Sinopharm da China e outra da AstraZeneca e da Universidade de Oxford. A da Sinovac Biotech, da China, deve se tornar a terceira no final deste mês. Os ensaios de fase 1 e 2 normalmente testam a segurança de um medicamento antes de entrar nos ensaios de fase 3, que testam sua eficácia em um grupo maior de voluntários. Os testes em humanos da vacina do Instituto Gamaleya começaram em 18 de junho, com nove voluntários recebendo uma dose e outros nove testando a dose potencial de reforço. O grupo não apresentou efeitos colaterais significativos e deve ser liberado do hospital na quarta-feira, informou a RIA no domingo, citando um diretor da Universidade Sechenov em Moscou, onde ocorreu a avaliação. Outros 20 voluntários receberam a vacina em um hospital militar em 23 de junho.

A chinesa SinoVac está iniciando os testes da fase 3 de sua potencial vacina contra o novo coronavírus, informou a farmacêutica nessa segunda-feira (6), tornando-se uma das três empresas a avançar aos estágios finais da corrida para desenvolver uma imunização contra a doença.Voluntários começarão a ser recrutados neste mês. A vacina será testada no Brasil, em um estudo com 9 mil voluntários liderado pelo Instituto Butantã, vinculado ao governo do estado de São Paulo. Na sexta-feira (3), a Agência Nacional de Vigilância Sanitária (Anvisa) autorizou a realização dos testes, que serão feitos em 12 centros de pesquisa localizados, além de São Paulo, em mais quatro estados e no Distrito Federal. Sobre a posição dos ensaios realizados com candidatas a vacina em todo o mundo, o documento mais recente da Organização Mundial da Saúde (OMS), divulgado nessa segunda-feira, informou que a SinoVac está na fase 3. A vacina experimental para covid-19 da AstraZeneca, desenvolvida por pesquisadores da Universidade de Oxford e que já está sendo testada no Brasil, em estudo liderado pela Universidade Federal de São Paulo (Unifesp), e a da Sinopharm são as outras candidatas em fase 3, o estágio final. A SinoVac está construindo uma fábrica de vacinas, que deverá ficar pronta neste ano e ser capaz de produzir até 100 milhões de doses anualmente. Os ensaios de fase 1 e fase 2 normalmente testam a segurança de um medicamento antes de entrar nos de fase 3, que testam sua eficácia. Existem 19 ensaios de vacinas em avaliação clínica, e centenas estão sendo desenvolvidas e testadas em todo o mundo para conter a pandemia de covid-19, doença respiratória que já matou milhares de pessoas e devastou a economia global.
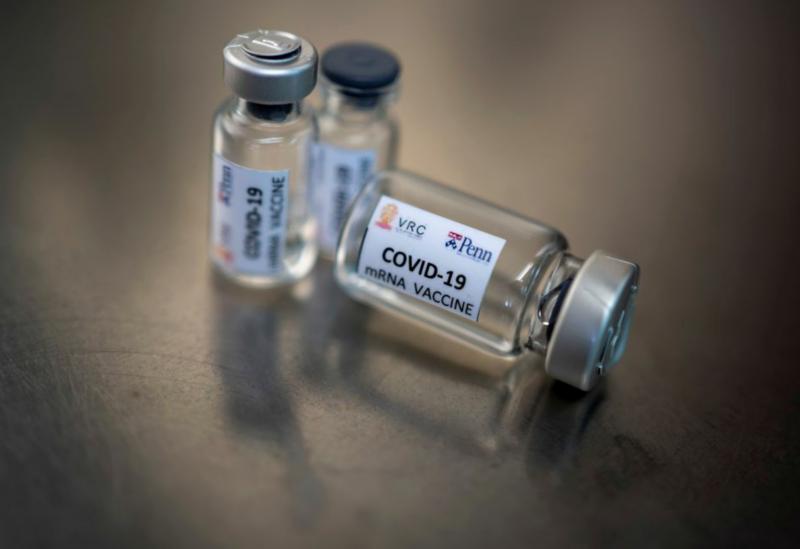
A vacina contra o covid-19, desenvolvida pela Universidade de Oxford, na Inglaterra, com testes no Brasil, poderá ficar disponível à população ainda este ano. A afirmação foi feita por Maria Augusta Bernardini, diretora-médica do grupo farmacêutico Astrazeneca. O grupo anglo-sueco participa das pesquisas da universidade inglesa em parceria com Universidade Federal de São Paulo (Unifesp). “Esperamos ter dados preliminares quanto a eficácia real já disponíveis em torno de outubro, novembro”, disse Bernardini. Segundo ela, apesar de os voluntários serem acompanhados por um ano, existe a possibilidade de distribuir a vacina à população antes desse período. “Vamos sim analisar, em conjunto com as entidades regulatórias mundiais, se podemos ter uma autorização de registro em caráter de exceção, um registro condicionado, para que a gente possa disponibilizar à população antes de ter uma finalização completa dos estudos”, acrescentou, destacando que os prazos podem mudar de acordo com a evolução dos estudos. Segundo ela, a Agência Nacional de Vigilância Sanitária (Anvisa) tem se mostrado disposta a colaborar. A vacina está atualmente na fase três de testes. Isso significa, de acordo a Unifesp, que a vacina se encontra entre os estágios mais avançados de desenvolvimento. O Brasil é o primeiro país fora do Reino Unido a iniciar testes com a vacina desenvolvida pela Universidade de Oxford e um dos motivos que levaram à escolha foi o fato de a pandemia estar em ascensão no país. “O Brasil é um grande foco de crescimento, de mortalidade, o que nos coloca como ambiente propício para demonstrar o potencial efeito de uma vacina. Para isso precisamos ter o vírus circulante na população e esse é o cenário que estamos vivendo”, disse Bernardini. Ela participou, hoje (29), de uma conversa, transmitida ao vivo pela internet, com o embaixador do Reino Unido no Brasil, Vijay Rangarajan. A diretora-médica da Astrazeneca também destacou que a atuação de pesquisadores brasileiros em Oxford e sua reputação foi outro fator influenciador para trazer a pesquisa para o Brasil. “Isso fortaleceu a imagem a reputação científica do Brasil, além de facilitar, trazer com agilidade o estudo em termos de execução”.
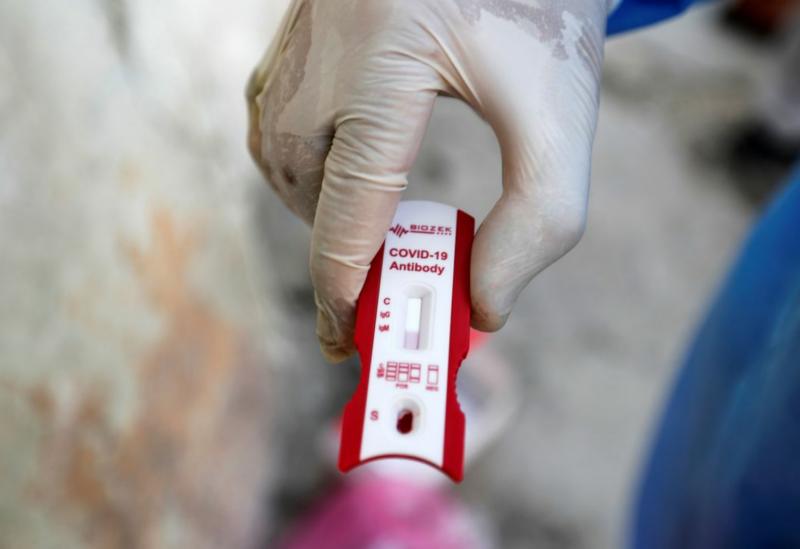
O Brasil fechou acordo para disponibilização no futuro de doses de uma vacina que está sendo testada para o tratamento da covid-19. O medicamento está sendo desenvolvido em uma iniciativa conjunta da Universidade de Oxford e de um laboratório no Reino Unido e já está sendo testado no país. O acordo prevê a produção de 100 milhões de doses de vacina por meio da aquisição de insumos e transferência de tecnologia para produção no país. Dois lotes, de 15,2 milhões de unidades cada, serão disponibilizados em dezembro de 2020 e janeiro de 2021, totalizando cerca de 30 milhões de doses, ao custo de US$ 127 milhões. Caso seja comprovada a eficácia deste tratamento, o Brasil poderá disponibilizar mais 70 milhões de doses, por cerca de US$ 160 milhões. Em entrevista coletiva em Brasília, o secretário executivo do Ministério da Saúde, Élcio Franco, justificou a opção por assumir o risco da pesquisa, mesmo sem a comprovação da eficácia do medicamento. “O risco é necessário devido à urgência de busca de solução efetiva para as demandas de saúde pública. Consideramos um avanço para a tecnologia nacional e uma amostra do esforço do governo de encontrar soluções para a população brasileira." O secretário de Vigilância em Saúde, Arnaldo de Medeiros, destacou a situação promissora deste tratamento. “A vacina já está na fase 3, em fase clínica. O Brasil é representante do conjunto de nações que estão testando a vacina. A gente tem uma oportunidade de produzirmos e avançarmos com a oferta desta parceria e encomenda tecnológica. É óbvio que toda e qualquer entrega à população será feita com respeito aos critérios farmacológicos e clínicos e da segurança à população”, declarou. Segundo o secretário, em caso de decisão pelo uso da vacina serão priorizados os grupos de risco, como idosos e pessoas com comorbidades, além de profissionais de saúde e trabalhadores da segurança pública. Caso não seja comprovada a eficácia, o secretário de Vigilância em Saúde informou que não haverá aplicação da vacina, mas que permanece a transferência de tecnologia prevista no acordo para continuar avaliando soluções de tratamento. De acordo com o Ministério da Saúde, há 460 projetos de pesquisa aprovados sobre diferentes aspectos relacionados à covid-19, de tratamentos ao entendimento da doença. Há também 114 ensaios clínicos e 44.262 participantes dessas iniciativas.
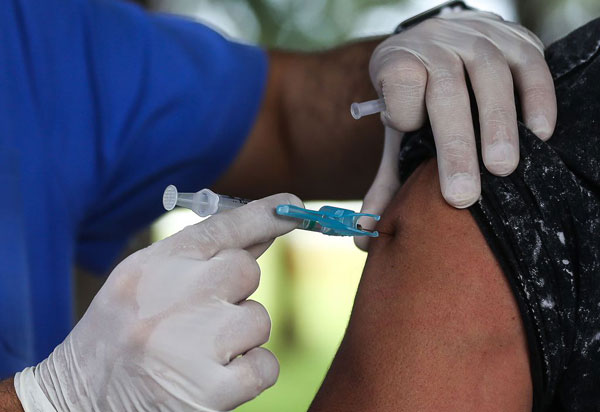
Conforme informou a Fundação Lemann, em comunicado divulgado nesta segunda-feira (22), no último final de semana (20 e 21 de junho), foi celebrado o início dos testes em São Paulo da potencial vacina contra a Covid-19 desenvolvida pela Universidade Oxford. De acordo com informações da CNN, o Grupo Fleury divulgou sua participação na seleção de dois mil voluntários brasileiros que receberão doses da vacina. O composto desenvolvido pela Universidade de Oxford é considerado um dos mais avançados entre todas as vacinas em teste para combater o novo coronavírus. O imunizante já demonstrou segurança em etapas anteriores e agora se encontra na fase três de testes, na qual uma grande quantidade de pessoas receberá doses para verificar sua eficácia em impedir o contágio.
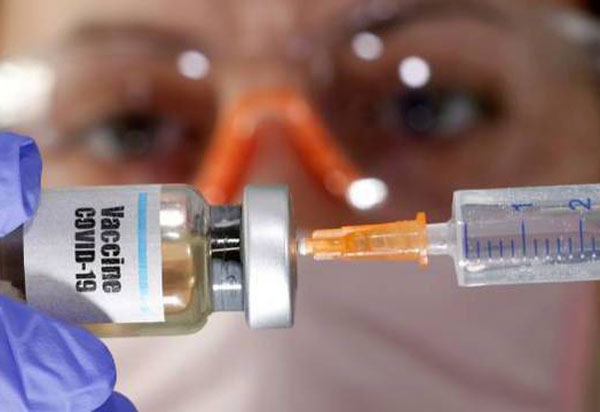
A Anvisa publicou na terça-feira (2/6), em edição extra do Diário Oficial da União (D.O.U.), a autorização para realização de um estudo clínico no Brasil para testar uma potencial vacina desenvolvida pela Universidade de Oxford, no Reino Unido, para prevenir a Covid-19. O pedido de autorização foi feito pela empresa Astrazeneca do Brasil Ltda., que submeteu os dados e as informações sobre a vacina para avaliação da Agência. Trata-se de um estudo controlado randomizado de fase III para determinar a segurança, a eficácia e a imunogenicidade da vacina ChAdOx1 nCoV-19 não replicante. Os estudos iniciais não clínicos em animais e os estudos clínicos de fase 1 em humanos para avaliar a segurança da vacina foram realizados na Inglaterra e os resultados demonstraram que o seu perfil de segurança foi aceitável. A vacina ChAdOx1 nCoV-19, conhecida como AZD1222, usa um vetor viral baseado em uma versão enfraquecida do resfriado comum (adenovírus) contendo o material genético da proteína spike Sars-CoV-2. O vetor de adenovírus recombinante (ChAdOx1) foi escolhido para gerar uma forte resposta imune a partir de uma dose única sem causar uma infecção contínua no indivíduo vacinado.