Pressione Enter para pesquisar ou ESC para sair
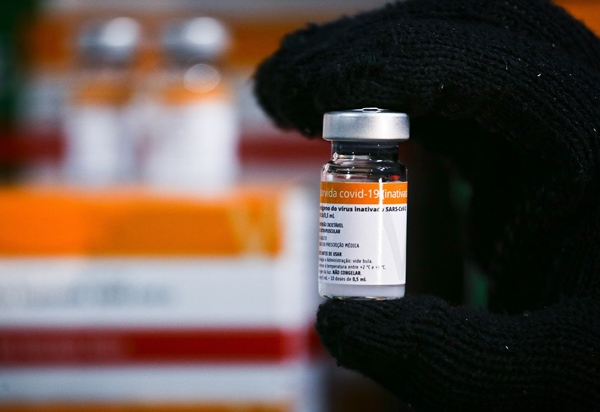
O Instituto Butantan, ligado à Secretaria de Ciência, Pesquisa e Desenvolvimento em Saúde do Governo de São Paulo, vai entregar ao Ministério da Saúde um milhão de novas doses da CoronaVac para a imunização de crianças entre 3 e 5 anos de idade contra a Covid-19 no país nesta quinta-feira (10). As doses adquiridas fazem parte do aditivo do contrato de compra de 10 milhões de vacinas, realizada no início deste ano, e foram produzidas no complexo fabril do instituto, em São Paulo, com IFA (Insumo Farmacêutico Ativo) importado da farmacêutica Sinovac, na China. Em setembro, o Butantan já havia entregue um milhão de doses ao PNI, após a aprovação do uso da CoronaVac pela Agência Nacional de Vigilância Sanitária (ANVISA) para o público de crianças de 3 a 5 anos. Para a imunização com as duas doses previstas para o esquema vacinal completo de crianças dessa faixa etária é necessário um total de quase 12 milhões de doses de vacinas contra Covid-19.
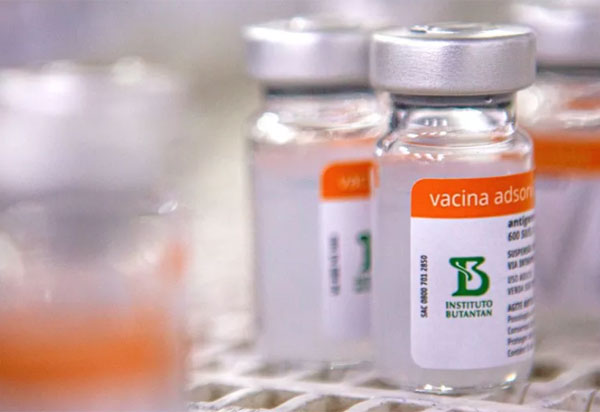
Nesta quarta-feira (13), a Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, em reunião colegiada, a extensão de uso emergencial pediátrico da vacina CoronaVac para a faixa etária de 3 a 5 anos. O esquema vacinal aprovado segue o mesmo protocolo que é aplicado em crianças maiores de 6 anos e adultos, com mesma dosagem e intervalo de 28 dias entre aplicações. Após aprovação pela Anvisa, o Butantan espera agora que o imunizante seja incorporado ao Programa Nacional de Imunizações (PNI) do Ministério da Saúde, de acordo com a demanda necessária e mediante contratação. A CoronaVac atendeu às necessidades do povo brasileiro nos momentos mais críticos da pandemia de Covid-19, sendo o primeiro imunizante a ser aplicado no país e nas populações mais vulneráveis naquele contexto, os idosos e profissionais da saúde. Agora, a vacina produzida em parceria com a farmacêutica Sinovac poderá ser novamente utilizada para proteção dos mais expostos ao Sars-Cov-2 – especialmente com a circulação de novas variantes mais transmissíveis da ômicron, que têm causado aumento de casos no Brasil. No país, 15% das internações ocasionadas por Covid-19 são de crianças menores de 5 anos. Além disso, a média de óbitos nesta população é de duas mortes por dia, o que as classifica como o grupo mais vulnerável à doença neste momento. A eficácia da CoronaVac em crianças de 3 a 5 anos foi comprovada não só por estudos clínicos controlados, como também por dados epidemiológicos do mundo real, que demonstram a sua efetividade. No Chile, uma pesquisa revisada por pares e publicada na Nature, feita com 500 mil crianças, mostrou que o imunizante forneceu proteção de 69% contra internação em Unidade de Terapia Intensiva (UTI) e 64,6% contra hospitalização por Covid-19.
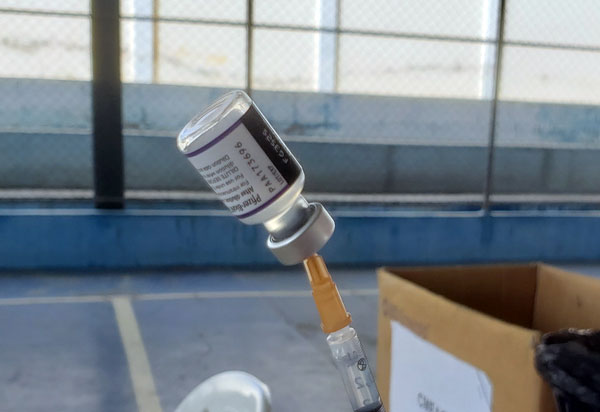
Receber uma dose de reforço da vacina da Pfizer após duas doses de CoronaVac produz uma proteção mais efetiva contra a variante Ômicron do que uma terceira aplicação da CoronaVac, indica um estudo divulgado hoje (5) pela Fundação Oswaldo Cruz (Fiocruz). O trabalho avaliou dados do e-SUS, do Sistema de Informação de Vigilância Epidemiológica da Gripe (Sivep-Gripe) e do Programa Nacional de Imunizações (PNI). Os dados abrangem de 6 de setembro de 2021 a 10 de março de 2022, e foram divididos em dois períodos, de 6 de setembro de 2021 a 14 de dezembro de 2021, quando a variante Delta era a dominante no Brasil; e de 25 de dezembro de 2021 a 10 de março de 2022, quando havia maior circulação da variante Ômicron. Para avaliar a efetividade da dose de reforço em pessoas vacinadas com duas doses de CoronaVac foram desenhados três cenários. No primeiro, foram analisadas pessoas que receberam as duas doses da vacina produzida no Instituto Butantan e não reforçaram a imunização nos seis meses seguintes. Os pesquisadores calcularam que a efetividade de apenas doses contra infecções sintomáticas durante o período de maior circulação da variante Ômicron foi de 8,1%, enquanto a proteção contra desfechos graves da doença chegou a 57%. No segundo cenário, foram avaliados casos em que as pessoas receberam uma dose de reforço também de CoronaVac, o que produziu uma proteção adicional considerada limitada pelos pesquisadores. A efetividade contra infecções sintomáticas foi de 15%, e contra casos graves, de 71,3%. O terceiro cenário, em que a dose de reforço foi com a vacina da Pfizer, apresentou os maiores percentuais de efetividade: de 56,8% contra infecções sintomáticas e de 85,5% contra casos graves. Além disso, o estudo mostrou que, 90 dias após a dose de reforço, a proteção contra casos graves não caiu, o que foi observado na vacinação com três doses da CoronaVac.
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu solicitação do Instituto Butantan para incluir a faixa etária de 3 a 5 anos na indicação da vacina Coronavac. O prazo de avaliação para esse novo pedido é de até sete dias úteis e começa a contar a partir de segunda-feira (14). “A análise técnica será feita pela Anvisa de forma rigorosa e com toda a cautela necessária para esse público específico”, informou a Agência, após receber a solicitação na noite dessa sexta-feira (11). Caso o pedido seja deferido pela Anvisa, a Coronavac pode ser a primeira vacina contra o coronavírus autorizada para crianças a partir dos 3 anos de idade. Atualmente, a imunização pediátrica contra a covid-19 é permitida partir dos 5 anos, mas somente a vacina da Pfizer tem autorização para crianças dessa idade. A partir dos 6 anos, elas podem receber a Pfizer ou Coronavac.
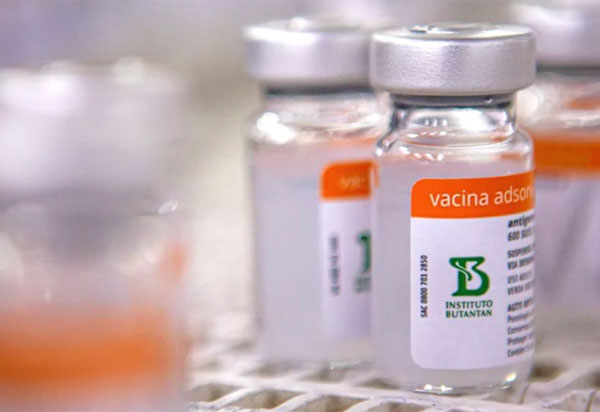
O Instituto Butantan vai entregar um lote com 10 milhões de doses da vacina CoronaVac ao Ministério da Saúde amanhã cedo (17). A informação foi confirmada hoje (16) pelo presidente do Butantan, Dimas Covas. As doses, já envasadas e certificadas, serão utilizadas para a que a vacinação de crianças avance em outros estados brasileiros.
 “Nós entregaremos a totalidade das 10 milhões de doses que já saem amanhã para os depósitos do Ministério da Saúde. O contrato foi assinado e, portanto, a liberação será imediata. Neste momento, estamos nos preparando para fazer esta entrega amanhã de manhã”, explicou Covas. A vacina CoronaVac contra a covid-19 é produzida pelo Instituto Butantan e o laboratório chinês Sinovac. A vacina é segura e foi aprovada pela Agência Nacional de Vigilância Sanitária (Anvisa) para ser aplicada em pessoas acima dos 6 anos. Nos próximos dias, o Instituto Butantan pretende solicitar à Anvisa que essa vacina possa também ser aplicada em crianças acima dos 3 anos.
“Nós entregaremos a totalidade das 10 milhões de doses que já saem amanhã para os depósitos do Ministério da Saúde. O contrato foi assinado e, portanto, a liberação será imediata. Neste momento, estamos nos preparando para fazer esta entrega amanhã de manhã”, explicou Covas. A vacina CoronaVac contra a covid-19 é produzida pelo Instituto Butantan e o laboratório chinês Sinovac. A vacina é segura e foi aprovada pela Agência Nacional de Vigilância Sanitária (Anvisa) para ser aplicada em pessoas acima dos 6 anos. Nos próximos dias, o Instituto Butantan pretende solicitar à Anvisa que essa vacina possa também ser aplicada em crianças acima dos 3 anos.

Em reunião realizada nesta quinta-feira (20/1), a Diretoria Colegiada da Anvisa aprovou, por unanimidade, o uso pediátrico da CoronaVac. A autorização de uso emergencial para a inclusão de nova faixa etária em bula foi concedida especificamente para o público compreendido entre 6 e 17 anos, crianças e adolescentes não imunocomprometidos, baseada em estudos realizados em diversos países, como China e Chile, e apresentados pelo Instituto Butantan no processo. Para esse público, a dose aprovada do imunizante, produzido a partir de vírus inativado, é a mesma usada para adultos (600 SU em 0,5 ml), com um intervalo de 28 dias entre a primeira e a segunda aplicação. No decorrer do processo foram avaliados estudos clínicos de fase I e II, dados preliminares dos estudos de eficácia, segurança e imunogenicidade (fase III) realizados com 14 mil crianças em cinco diferentes países, e de estudos de efetividade (fase IV) realizados com milhões de crianças no Chile. As evidências científicas disponíveis até o momento sugerem que há benefícios e segurança para a utilização da vacina na população pediátrica. A autorização levou em conta, também, a necessidade de ampliar as alternativas disponíveis para essa faixa etária. Esclarece-se, no entanto, que a decisão sobre a incorporação da CoronaVac para essa nova faixa etária no Programa Nacional de Imunizações (PNI) cabe ao Ministério da Saúde. No Brasil, até o momento, a análise de causalidade acerca de reações adversas demonstra que a vacina CoronaVac não está relacionada a nenhum óbito dentre os públicos para os quais estava disponível até então e os eventos adversos graves são considerados raros ou raríssimos. Já no cenário internacional, nos países em que a CoronaVac já vem sendo aplicada no público de 2 a 17 anos, os dados demonstram que 86% dos eventos adversos registrados nessa faixa etária são do tipo não graves. Ainda assim, a aprovação para o público de 6 a 17 anos no Brasil foi condicionada ao monitoramento constante e à comunicação dos eventos adversos que venham a ser registrados, além da manutenção de um plano de gerenciamento para minimizar riscos, que contemple a execução de estudos de segurança pós-autorização.

Após autorizar, ainda em dezembro, o uso do imunizante da Pifzer contra a covid-19 em crianças de 5 a 11 anos de idade, a Agência Nacional de Vigilância Sanitária (Anvisa) analisa um pedido do Instituto Butantan para uso da CoronaVac em crianças e adolescentes de 3 a 17 anos. O Butantan, fabricante da CoronaVac no Brasil, pediu autorização da Anvisa para uso do imunizante nesse público em dezembro, mas à época a Anvisa cobrou mais dados do instituto afirmando que os fornecidos não eram suficientes para a decisão. Ontem (6) a Anvisa teve uma série de reuniões sobre o assunto dividida em três etapas: a primeira contou com a apresentação de estudos de efetividade feitos pela Fundação Oswaldo Cruz (Fiocruz). Na sequência, os dados foram debatidos por especialistas externos convidados pela Anvisa, tais como representantes da Sociedade Brasileira de Infectologia (SBI), do Departamento de Infectologia da Sociedade Brasileira de Pediatria (SBP), da Sociedade Brasileira de Imunologia (SBI) e da Associação Brasileira de Saúde Coletiva (Abrasco). A equipe técnica da Anvisa se reuniu ainda com o Instituto Butantan, técnicos do Chile e da Sinovac, farmacêutica chinesa que desenvolveu o imunizante. De acordo com a agência reguladora, os encontros “são mais um passo na análise da vacina” e os dados apresentados “representam um avanço nos trabalhos”.
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu um novo pedido do Instituto Butantan indicando a aplicação da vacina CoronaVac em crianças e adolescentes com idades entre 3 e 17 anos. Em nota, a Anvisa explicou que, para a inclusão de “novos públicos na bula”, será necessário ao laboratório que conduza “estudos que demonstrem a relação de segurança e eficácia para determinada faixa etária”. “Este é o segundo pedido do laboratório para indicação do imunizante para essa faixa etária. O primeiro, apresentado em julho, foi avaliado pela Anvisa e negado devido à limitação de dados dos estudos apresentados naquele momento”, informou a Anvisa, que tem agora prazo de até 30 dias para avaliar a nova solicitação. A Anvisa lembrou, ainda, que a vacina CoronaVac tem autorização para uso emergencial no Brasil apenas para pessoas com 18 anos de idade ou mais. “A solicitação de ampliação de uso da vacina, ou seja, a inclusão de uma nova faixa etária, é feita pelo laboratório responsável pelo imunizante”, acrescentou a agência.
A farmacêutica chinesa Sinovac, parceira do Instituto Butantan no desenvolvimento da vacina CoronaVac, contra a Covid-19, anunciou nesta terça (9) que os resultados preliminares dos ensaios clínicos de fase 3 que estão sendo realizados na África do Sul, Chile, Malásia e Filipinas comprovam que o imunizante é seguro para crianças e adolescentes de três a 17 anos. Desde outubro de 2021, 2.140 jovens de seis meses a 17 anos participam do estudo, que é multicêntrico, randomizado, duplo-cego e controlado por placebo. Os primeiros resultados mostraram que a vacina tem um bom perfil de segurança entre participantes saudáveis com três a 17 anos – para os mais novos, a pesquisa continua em andamento. Os resultados dos dados de segurança revelaram que a incidência de efeitos adversos após a segunda dose da CoronaVac foi muito menor do que quando da primeira dose. Os efeitos adversos locais e sistêmicos envolveram principalmente dor no local da injeção, dor de cabeça e febre. Não ocorreram efeitos adversos graves suspeitos e inesperados. O estudo fornecerá uma base científica mais sólida para que os países realizem com segurança a imunização de suas crianças e adolescentes contra o SARS-CoV-2. Várias nações, incluindo Chile, Equador, El Salvador, Colômbia, Camboja e Indonésia, já aprovaram o uso de CoronaVac para pessoas saudáveis na faixa de três a 17 anos. Na China, até o final de outubro mais de 110 milhões de doses da vacina do Butantan e da Sinovac foram administradas a menores de 18 anos.
De acordo com informações da Secretaria de Saúde do Estado da Bahia (Sesab), 4.161 pessoas na Bahia receberam doses dos lotes da vacina Sinovac/Coronavac que a Agência Nacional de Vigilância Sanitária (Anvisa) determinou que estão proibidos de serem distribuídos e utilizados por até 90 dias. Dos 42 lotes comprometidos, três deles foram recebidos pela Bahia nos dias 27 de julho e 1º de setembro. Em nota, a Sesab informou que a Diretoria de Vigilância Epidemiológica\Coordenação Estadual de Imunização estava aguardando parecer da Anvisa sobre a questão, para saber se seriam desinterditadas e não seria necessária a devolução. "Em caso de confirmada a interdição, faríamos a logística reversa, ou seja, a devolução", diz a nota. A reportagem do Agora Sudoeste entrou em contato com o secretário de Saúde de Brumado, Cláudio Feres, para obter informações do sobre o assunto. O gestor da pasta informou que o município não recebeu esse lote da vacina em questão.
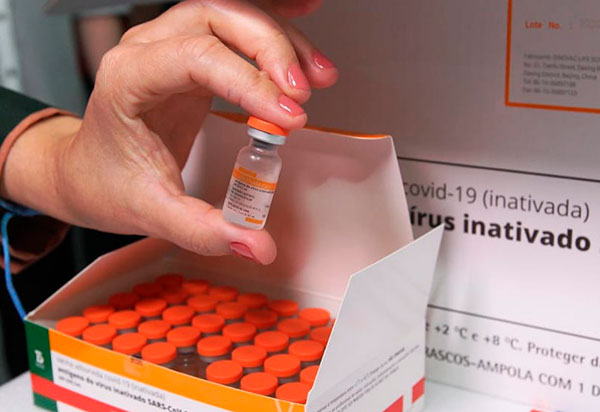
A Agência Nacional de Vigilância Sanitária (Anvisa) determinou o recolhimento de alguns lotes da vacina CoronaVac, contra a covid-19, que foram interditados após constatação de que “dados apresentados pelo laboratório não comprovam a realização do envase da vacina em condições satisfatórias de boas práticas de fabricação”.
 A determinação foi anunciada hoje (22) por meio da Resolução (RE) 3.609, que determinou o recolhimento dos lotes da CoronaVac que já haviam sido interditados de forma cautelar pela Resolução (RE) 3.425, de 4 de setembro de 2021. No dia 3 de setembro, a agência foi comunicada pelo Instituto Butantan que o parceiro na fabricação vacina CoronaVac, o laboratório Sinovac, havia enviado para o Brasil 25 lotes na apresentação frasco-ampola (monodose e duas doses), totalizando 12.113.934 doses, que foram envasados em instalações não inspecionadas pela Anvisa. Diante da situação, e “considerando as características do produto e a complexidade do processo fabril, já que vacinas são produtos estéreis (injetáveis) que devem ser fabricados em rigorosas condições assépticas”, a Anvisa adotou medida cautelar com o objetivo de mitigar um potencial risco sanitário. Em nota divulgada há pouco, a agência informa que, desde a interdição cautelar, avaliou todos os documentos encaminhados pelo Instituto Butantan, “dentre os quais os emitidos pela autoridade?sanitária chinesa”. “Os documentos encaminhados consistiram em formulários de não conformidades que reforçaram as preocupações quanto às práticas assépticas e à rastreabilidade dos lotes”, detalha a nota.
A determinação foi anunciada hoje (22) por meio da Resolução (RE) 3.609, que determinou o recolhimento dos lotes da CoronaVac que já haviam sido interditados de forma cautelar pela Resolução (RE) 3.425, de 4 de setembro de 2021. No dia 3 de setembro, a agência foi comunicada pelo Instituto Butantan que o parceiro na fabricação vacina CoronaVac, o laboratório Sinovac, havia enviado para o Brasil 25 lotes na apresentação frasco-ampola (monodose e duas doses), totalizando 12.113.934 doses, que foram envasados em instalações não inspecionadas pela Anvisa. Diante da situação, e “considerando as características do produto e a complexidade do processo fabril, já que vacinas são produtos estéreis (injetáveis) que devem ser fabricados em rigorosas condições assépticas”, a Anvisa adotou medida cautelar com o objetivo de mitigar um potencial risco sanitário. Em nota divulgada há pouco, a agência informa que, desde a interdição cautelar, avaliou todos os documentos encaminhados pelo Instituto Butantan, “dentre os quais os emitidos pela autoridade?sanitária chinesa”. “Os documentos encaminhados consistiram em formulários de não conformidades que reforçaram as preocupações quanto às práticas assépticas e à rastreabilidade dos lotes”, detalha a nota.
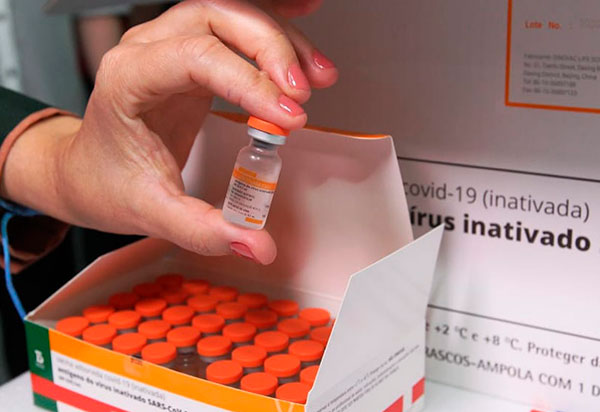
Informações preliminares do estudo CovacManaus, realizado na capital amazonense, mostram que a CoronaVac, vacina da farmacêutica chinesa Sinovac contra a covid-19 garante proteção contra a doença superior a 90% em pessoas com comorbidades. As informações são do Instituto Butantan, que produz o imunizante no Brasil. A pesquisa está sendo feita com 5 mil profissionais da educação e da segurança pública da rede estadual de Manaus, com idades entre 18 e 49 anos. Do total desse público vacinado com o imunizante, somente 2,6% tiveram infecções causadas pelo SARS-CoV-2. O índice de hospitalizações pela doença foi de 0,1%, e o de admissões em Unidades de Terapia Intensiva (UTIs) foi de 0,04%. Um óbito foi confirmado, configurando uma porcentagem de 0,02% da amostra. “A efetividade da CoronaVac foi superior a 97% contra infecções, hospitalizações, internações em UTI [unidades de terapia intensiva] e mortes. Outro indicador relevante é que, entre os vacinados, 91% apresentaram anticorpos detectáveis após tomarem a primeira dose, e 99,8% após a segunda dose”, destacou o Butantan em nota.
 Entre as principais comorbidades apresentadas pelos voluntários que participam do estudo estão obesidade (72%), diabetes (54%), hipertensão arterial (36%) e imunossupressão (27%).
Entre as principais comorbidades apresentadas pelos voluntários que participam do estudo estão obesidade (72%), diabetes (54%), hipertensão arterial (36%) e imunossupressão (27%).
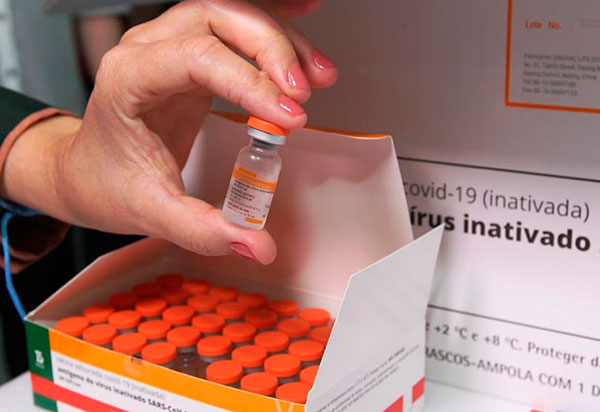
Por determinação da Agência Nacional de Vigilância Sanitária (Anvisa), a partir deste sábado (4), 42 lotes da vacina Sinovac/Coronavac estão proibidos de serem distribuídos e utilizados por até 90 dias. Deste total, o Ministério da Saúde já havia distribuído 25 lotes para todo o Brasil, sendo três deles recebidos pela Bahia nos dias 27 de julho e 1º de setembro. A medida cautelar publicada no Diário Oficial da União foi motivada pelo envase ter ocorrido em uma planta fabril na China que não foi inspecionada e aprovada para Autorização de Uso Emergencial no Brasil. A Bahia recebeu 575.980? doses da vacina Sinovac/Coronavac, sendo 571.280 em 1º de setembro e 4.700 em 27 de julho. Os quantitativos referem-se aos lotes 202107101H, 202107102H e L202106038. Deste total, 234.380? já tinham sido entregues a 294 municípios. Todos já foram comunicados para interromper a vacinação dos lotes específicos da Sinovac/Coronavac. As pessoas imunizadas com estes lotes devem aguardar a orientação do Ministério da Saúde, por meio do Programa Nacional de Imunizações (PNI). Em documento enviado à Anvisa, o Instituto Butantan assegura que os lotes apontam segurança e qualidade das vacinas produzidas na fábrica que ainda não foi inspecionada. É preciso ressaltar que apenas os lotes especificados não devem ser utilizados. Os demais tem segurança, qualidade e eficácia comprovada.

De acordo com trabalho publicado na plataforma medRxiv e ainda em processo de revisão, de autoria de pesquisadores das universidades federais da Bahia e de Ouro Preto, da Universidade de Brasília (UnB), da Universidade Estadual do Rio de Janeiro (Uerj) e da London School of Hygiene & Tropical Medicine e da Fundação Oswaldo Cruz (Fiocruz), com dados de 60 milhões de brasileiros vacinados entre 18 de janeiro e 30 de junho, o estudo avaliou a efetividade das vacinas CoronaVac e AstraZeneca para prevenir casos graves de covid-19, hospitalizações, admissão em UTIs e mortes. Segundo o resultado, no caso da vacina desenvolvida pelo Instituto Butantan, a CoronaVac, com o esquema vacinal completo, a pessoa imunizada tem 74% menos risco de morte. Com a AstraZeneca, o percentual é acima de 90%. Segundo informações da da Agência Brasil, considerando todas as faixas etárias dos vacinados, entre os que tomaram duas doses da CoronaVac, 54,2% apresentaram risco menor de infecção pelo novo coronavírus, 72,6% menos risco de hospitalização, 74,2% menos risco de admissão na UTI, e 74% menos risco de morte. Para quem tomou apenas uma dose, o risco de infecção caiu pela metade, além disso, o estudo apontou 26,5% menos risco de hospitalização, 28,1% menos risco de admissão em UTI e 29,4% menos risco de morte.Com a AstraZeneca, os que completaram a imunização com duas doses apresentaram 70% menos risco de infecção, 86,8% menos risco de internação, 88,1% menos risco de admissão na UTI e 90,2% menos risco de morte.
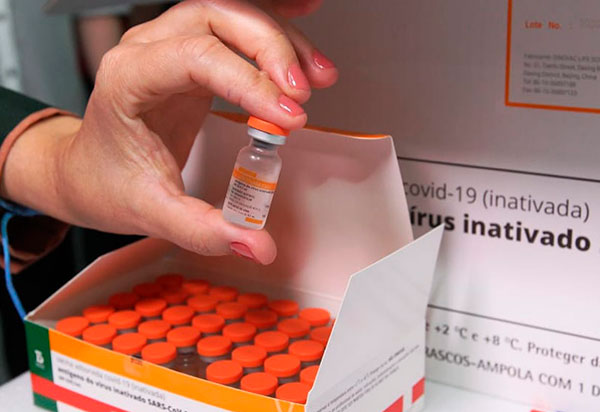
A Agência Nacional de Vigilância Sanitária (Anvisa) rejeitou o pedido do Instituto Butantan para o uso da vacina CoronaVac em crianças e adolescentes de 3 a 17 anos.
 Em reunião extraordinária realizada nesta quarta-feira (18), a diretoria colegiada da agência avaliou que, com as informações apresentadas pelo Butantan, não é possível concluir sobre a eficácia e a segurança da dose nessa faixa etária. “Os dados de imunogenicidade deixam incertezas sobre a duração da proteção conferida pelo imunizante”, informou a Anvisa, por meio de nota. De acordo com a agência, o perfil de segurança da vacina também não permite concluir quais os riscos para crianças e adolescentes – em grande parte, devido ao número considerado insuficiente de participantes nos estudos. “Faltaram ainda dados que considerassem a vacinação em faixas etárias específicas. Também não é conhecida a eficácia ou a capacidade de indução de resposta imune pela vacina em crianças com comorbidades e imunossuprimidas.” Para prosseguir com a solicitação de inclusão da faixa etária de 3 a 17 anos, o Butantan, segundo a Anvisa, precisa apresentar informações pendentes e submeter um novo pedido à agência. A CoronaVac recebeu autorização temporária de uso de emergencial por parte da Anvisa em janeiro. A aprovação das doses sob essa condição permanece enquanto perdurar a situação de emergência em saúde pública decorrente da pandemia de covid-19 no Brasil. Atualmente, a vacina da Pfizer é a única aprovada para crianças e adolescentes de 12 a 17 anos. Já a farmacêutica Janssen, que oferece imunização contra a doença em dose única, recebeu autorização para a condução de estudos com menores de 18 anos no Brasil.
Em reunião extraordinária realizada nesta quarta-feira (18), a diretoria colegiada da agência avaliou que, com as informações apresentadas pelo Butantan, não é possível concluir sobre a eficácia e a segurança da dose nessa faixa etária. “Os dados de imunogenicidade deixam incertezas sobre a duração da proteção conferida pelo imunizante”, informou a Anvisa, por meio de nota. De acordo com a agência, o perfil de segurança da vacina também não permite concluir quais os riscos para crianças e adolescentes – em grande parte, devido ao número considerado insuficiente de participantes nos estudos. “Faltaram ainda dados que considerassem a vacinação em faixas etárias específicas. Também não é conhecida a eficácia ou a capacidade de indução de resposta imune pela vacina em crianças com comorbidades e imunossuprimidas.” Para prosseguir com a solicitação de inclusão da faixa etária de 3 a 17 anos, o Butantan, segundo a Anvisa, precisa apresentar informações pendentes e submeter um novo pedido à agência. A CoronaVac recebeu autorização temporária de uso de emergencial por parte da Anvisa em janeiro. A aprovação das doses sob essa condição permanece enquanto perdurar a situação de emergência em saúde pública decorrente da pandemia de covid-19 no Brasil. Atualmente, a vacina da Pfizer é a única aprovada para crianças e adolescentes de 12 a 17 anos. Já a farmacêutica Janssen, que oferece imunização contra a doença em dose única, recebeu autorização para a condução de estudos com menores de 18 anos no Brasil.
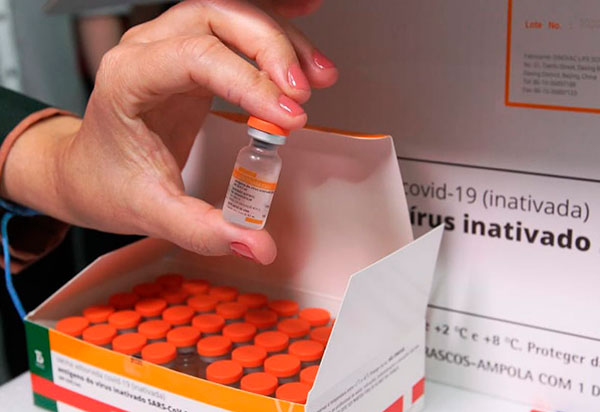
O governo de São Paulo entregou hoje (4) ao Programa Nacional de Imunizações (PNI) mais 2 milhões de doses da vacina contra covid-19 CoronaVac, produzida pelo Instituto Butantan em parceria com o laboratório chinês Sinovac. Com a nova entrega, as liberações chegam à marca de 64,8 milhões de doses fornecidas ao Ministério da Saúde desde 17 de janeiro, quando o uso emergencial do imunizante foi aprovado pela Agência Nacional de Vigilância Sanitária (Anvisa).
 Segundo informações do governo estadual, em julho foram entregues mais de 10 milhões de doses do imunizante, produzidos a partir de 6 mil litros de Ingrediente Farmacêutico Ativo (IFA) recebidos no dia 26 de junho. Na noite do último domingo (1º), o instituto recebeu uma carga de 2 mil litros de matéria-prima para produzir e entregar mais 4 milhões de doses da CoronaVac. As vacinas liberadas hoje fazem parte do segundo contrato firmado com o Ministério da Saúde, de 54 milhões de de doses do imunizante. O primeiro, de 46 milhões, foi concluído em 12 de maio.
Segundo informações do governo estadual, em julho foram entregues mais de 10 milhões de doses do imunizante, produzidos a partir de 6 mil litros de Ingrediente Farmacêutico Ativo (IFA) recebidos no dia 26 de junho. Na noite do último domingo (1º), o instituto recebeu uma carga de 2 mil litros de matéria-prima para produzir e entregar mais 4 milhões de doses da CoronaVac. As vacinas liberadas hoje fazem parte do segundo contrato firmado com o Ministério da Saúde, de 54 milhões de de doses do imunizante. O primeiro, de 46 milhões, foi concluído em 12 de maio.

A Bahia recebe nesta quarta-feira (04) 249.230 doses de vacina contra Covid-19. A primeira remessa, com 86.600 doses de Coronavac, chegou ao estado em um voo que pousou no aeroporto de Salvador às 9h20. O avião trazendo a segunda carga, com 165.630 doses da vacina produzida pela Pfizer/BioNTech, está previsto para pousar no aeroporto de Salvador às 16h50. As Coronavac serão destinadas para primeira e segunda aplicações, enquanto que a Pfizer/BioNTech para a primeira. As vacinas serão conferidas pela equipe da coordenação de imunização da Secretaria da Saúde do Estado e devem começar a ser enviadas para as regionais de saúde, de onde serão encaminhadas para os municípios nesta quinta-feira. Elas serão remetidas, exclusivamente, aos municípios que aplicaram 85% ou mais das doses anteriores. Esta foi uma decisão da Comissão Intergestores Bipartite (CIB), que é uma instância deliberativa da saúde e reúne representantes dos 417 municípios e o Estado. Com as duas remessas desta quarta, a Bahia chegará ao total de 11.582.140 doses de vacinas recebidas, sendo 4.120.500 da Coronavac; 5.586.900 da AstraZeneca/Oxford; 1.619.940 da Pfizer e 254.800 da Janssen.

Nesta segunda (26), o Instituto Butantan enviou ao Programa Nacional de Imunizações (PNI), do Ministério da Saúde, um novo lote contendo 1,5 milhão de doses da CoronaVac, vacina contra a Covid-19 produzida em parceria com a farmacêutica chinesa Sinovac. Com essa remessa, já são 60,149 milhões de doses do imunizante entregues ao governo federal desde meados de janeiro. Ainda nesta semana, sairão remessas de CoronaVac na quarta (28) e na sexta (30). Com isso, o Butantan encerra o envio das 10 milhões de doses produzidas a partir dos 6 mil litros de Insumo Farmacêutico Ativo (IFA) que chegaram da China no final de junho. Outros 12 mil litros de matéria-prima foram recebidos em 12/7, permitindo a produção de 20 milhões de doses, que em breve começarão a ser encaminhadas ao governo federal. A chegada de mais 12 mil litros de IFA enviados pela Sinovac está prevista para as próximas semanas. Dessa forma, o Butantan deve finalizar o contrato com o Ministério da Saúde para o fornecimento de 100 milhões de doses da CoronaVac antes do prazo estabelecido, que é o final de setembro.
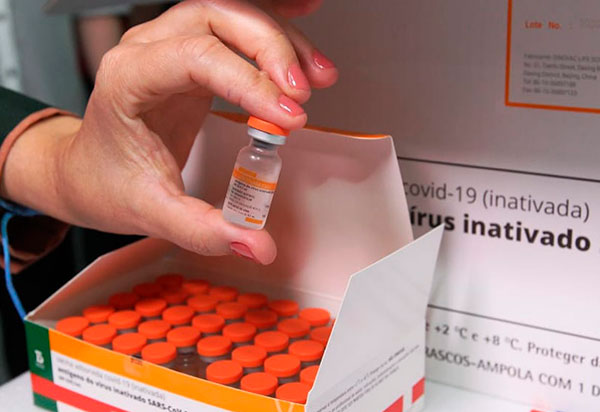
A Bahia receberá mais 613.060 doses de vacinas contra a Covid-19. Os imunizantes estão previstos pra chegar em três remessas. A primeira, com 255.300 doses da Coronavac e 63.600 da Oxford/AstraZeneca, chegará ao aeroporto de Salvador em um voo com pouso marcado para às 7h20 desta terça-feira (27). A segunda carga, com 150.250 imunizantes da Oxford/AstraZeneca, chegará em um voo com aterrissagem programada para 19h15, também de terça-feira. A terceira remessa, com 143.910 doses da Pfizer/BioNTech será trazida em um voo previsto para às 15h de quarta-feira (28). As vacinas devem começar a ser distribuídas ainda na terça-feira por via terrestre e também em aeronaves do Grupamento Aéreo da Polícia Militar e da Casa Militar do Governador, após conferência da equipe da Coordenação de Imunização do Estado. Elas serão remetidas, exclusivamente, aos municípios que aplicaram 85% ou mais das doses anteriores. Esta foi uma decisão da Comissão Intergestores Bipartite (CIB), que é uma instância deliberativa da saúde e reúne representantes dos 417 municípios e o Estado. Com estas novas remessas, a Bahia chegará ao total de 10.835.440 doses de vacinas recebidas, sendo 3.809.700 da Coronavac, 5.586.900 da Oxford/AstraZeneca, 1.184.040 da Pfizer e 254.800 da Janssen.
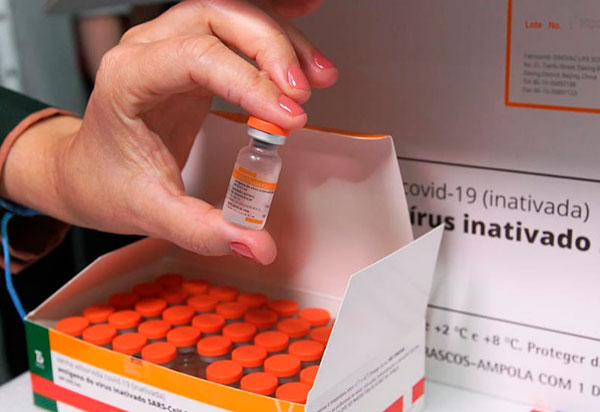
O Instituto Butantan recebeu nesta terça-feira (13) uma remessa de 12 mil litros de ingrediente farmacêutico ativo (IFA) para produção de vacina CoronaVac contra covid-19. A remessa, a maior até agora de matéria-prima vinda da China, é suficiente para o envase de 20 milhões de doses do imunizante.
 A carga saiu de Pequim no último domingo (11), fez escalada na Suíça, e chegou no Aeroporto Internacional de Guarulhos, na Grande São Paulo, às 4h30 de hoje. A preparação das vacinas para aplicação pelo Programa Nacional de Imunizações deve ser feita em um período de 15 a 20 dias. O imunizante será, então, disponibilizado para aplicação em todo o país. O Butantan já disponibilizou 53,1 milhões de doses da vacina elaborada em parceria com o laboratório chinês Sinovac. O instituto assinou dois contratos com o Ministério da Saúde para o fornecimento de 100 milhões de doses do imunizante até o final de agosto.
A carga saiu de Pequim no último domingo (11), fez escalada na Suíça, e chegou no Aeroporto Internacional de Guarulhos, na Grande São Paulo, às 4h30 de hoje. A preparação das vacinas para aplicação pelo Programa Nacional de Imunizações deve ser feita em um período de 15 a 20 dias. O imunizante será, então, disponibilizado para aplicação em todo o país. O Butantan já disponibilizou 53,1 milhões de doses da vacina elaborada em parceria com o laboratório chinês Sinovac. O instituto assinou dois contratos com o Ministério da Saúde para o fornecimento de 100 milhões de doses do imunizante até o final de agosto.
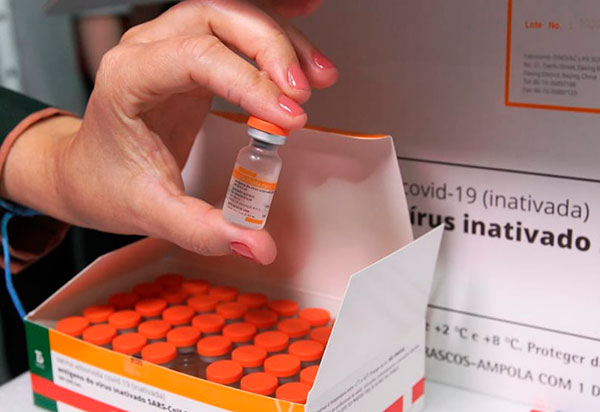
O Instituto Butantan liberou hoje (12) mais 1 milhão de doses da vacina contra o novo coronavírus ao Programa Nacional de Imunizações (PNI). Com essa remessa, o Butantan totaliza 46,112 milhões de doses disponibilizadas ao Ministério da Saúde desde o início deste ano e cumpre o primeiro contrato firmado com o governo federal em janeiro. 
 Segundo informações do governo de São Paulo, na próxima sexta-feira (14) começa a entrega das doses previstas no segundo contrato, que é de 54 milhões de vacinas. A primeira remessa será de 1,1 milhão de doses. “As vacinas entregues em maio foram produzidas a partir de 3 mil litros de insumos recebidos no dia 19 de abril. Assim que um novo lote de insumos da China chegar ao país, será possível retomar a produção e efetuar novas entregas do imunizante ao governo federal”, diz o governo estadual. De acordo com as informações, também serão entregues neste mês mais 30 milhões de doses da vacina contra a gripe para distribuição em todo o país.
Segundo informações do governo de São Paulo, na próxima sexta-feira (14) começa a entrega das doses previstas no segundo contrato, que é de 54 milhões de vacinas. A primeira remessa será de 1,1 milhão de doses. “As vacinas entregues em maio foram produzidas a partir de 3 mil litros de insumos recebidos no dia 19 de abril. Assim que um novo lote de insumos da China chegar ao país, será possível retomar a produção e efetuar novas entregas do imunizante ao governo federal”, diz o governo estadual. De acordo com as informações, também serão entregues neste mês mais 30 milhões de doses da vacina contra a gripe para distribuição em todo o país.

O Instituto Butantan entregou hoje (10) mais 2 milhões de doses da vacina contra o coronavírus CoronaVac. Com este lote, o instituto totaliza 45,1 milhões de doses do imunizante desenvolvido em parceria com o laboratório chinês Sinovac disponibilizadas para o Programa Nacional de Imunizações.
 A previsão é que o Butatan libere mais um milhão de doses na próxima quarta-feira (12), com concluindo o primeiro contrato assinado com o Ministério da Saúde para fornecimento de 46 milhões de doses da vacina. A estimativa inicial era de que esse total fosse disponibilizado até o final de abril. No entanto, a produção da CoronaVac tem sofrido atrasos devido à demora além do previsto para envio de matérias-primas pela China. O Butantan tem ainda um segundo contrato com o Ministério da Saúde para o fornecimento de 54 milhões de doses da vacina até 30 de agosto. O estado de São Paulo já imunizou completamente, com as duas doses de vacina contra o coronavírus, 4,7 milhões de pessoas, mais de 10% da população.
A previsão é que o Butatan libere mais um milhão de doses na próxima quarta-feira (12), com concluindo o primeiro contrato assinado com o Ministério da Saúde para fornecimento de 46 milhões de doses da vacina. A estimativa inicial era de que esse total fosse disponibilizado até o final de abril. No entanto, a produção da CoronaVac tem sofrido atrasos devido à demora além do previsto para envio de matérias-primas pela China. O Butantan tem ainda um segundo contrato com o Ministério da Saúde para o fornecimento de 54 milhões de doses da vacina até 30 de agosto. O estado de São Paulo já imunizou completamente, com as duas doses de vacina contra o coronavírus, 4,7 milhões de pessoas, mais de 10% da população.

O Instituto Butantan envia hoje (6) para o Ministério da Saúde um lote de mais 1 milhão de doses da vacina CoronaVac, desenvolvida pelo instituto em parceria com o laboratório chinês Sinovac. Desde o mês de janeiro, o Butantan entregou 42,05 milhões de doses da vacina ao Plano Nacional de Imunização (PNI), responsável pelo planejamento, coordenação e logística de distribuição do imunizante em todo o país. O Butantan informou que no último dia 19 recebeu nova remessa de 3 mil litros do ingrediente farmacêutico Ativo (IFA), matéria-prima importada necessária para a produção de novas doses da vacina contra o novo coronavírus. “Os insumos já foram processados, e as doses começam a ser liberadas a partir desta sexta [7] para completar as 46 milhões de doses do primeiro contrato firmado com o Ministério da Saúde”, diz o instituto, responsável pelo envase, a rotulagem, embalagem e inspeção de qualidade do imunizante. O instituto informou ainda que está negociando com a Sinovac o envio de mais um carregamento com 3 mil litros do IFA. “O Butantan trabalha para entregar mais 54 milhões de doses para a vacinação dos brasileiros até o dia 30 de agosto, totalizando 100 milhões de unidades contratadas até agora para a campanha contra a covid-19”.


Desde que começou a receber as vacinas contra a Covid-19, o município de Brumado já recebeu 11.187 doses, segundo atualização da Secretaria de Saúde da Bahia (Sesau). Com a primeira dose, foram realizadas 10.961 aplicações na Capital do Minério, ou seja, 98,00% das doses foram aplicadas. Em relacão a segunda dose, 67,5% do público prioritário foi imunizado.
A vacina contra a Covid-19 CoronaVac, produzida pelo Butantan em parceria com a farmacêutica chinesa Sinovac, provou-se eficaz contra a mutação D614G do vírus SARS-CoV-2, que predomina atualmente no mundo e é comum às linhagens B.1.1.28 (da qual derivam as variantes P.1, amazônica, e P.2, surgida no Rio de Janeiro) e B.1.1.33 (da qual deriva a variante N9, descoberta no Brasil recentemente). As informações foram divulgadas no último sábado (3) no site da Sinovac junto aos resultados consolidados dos quatro estudos clínicos de aplicação do imunobiológico realizados na China, no Brasil e na Turquia desde meados de 2020. As pesquisas demonstraram que, após a vacinação, a taxa de soroconversão (surgimento de anticorpo específico no sangue de um indivíduo) dos anticorpos neutralizantes contra 12 cepas do SARS-CoV-2 (incluindo a mutação D614G) variou de 80% a 100%. Foram avaliados 80 voluntários e as cepas CZ02, WZL, WGF, ZJY, SSH, JWL, ZYF, HAC, HJL, ZXZ, QHF e NOOR. Em março, o Butantan já havia divulgado dados iniciais de um estudo realizado em parceria com o Instituto de Ciências Biomédicas da Universidade de São Paulo, envolvendo 35 pessoas, e que apontava que a CoronaVac era eficaz contra as variantes P.1 e P.2 do novo coronavírus. As vacinas compostas de vírus inativado, como a CoronaVac, possuem todas as partes do vírus. Isso pode gerar uma resposta imune mais abrangente em relação ao que ocorre com vacinas que utilizam somente uma parte da proteína Spike (utilizada pelo coronavírus para infectar as células). Como a CoronaVac possui uma proteína Spike completa, pode levar a uma proteção mais efetiva contra as variantes que apresentam mutação nesse elemento.