Pressione Enter para pesquisar ou ESC para sair

A partir desta segunda-feira (8), profissionais de saúde da atenção primária que atuam no Sistema Único de Saúde (SUS) começam a receber a vacina contra a dengue desenvolvida pelo Instituto Butantan.
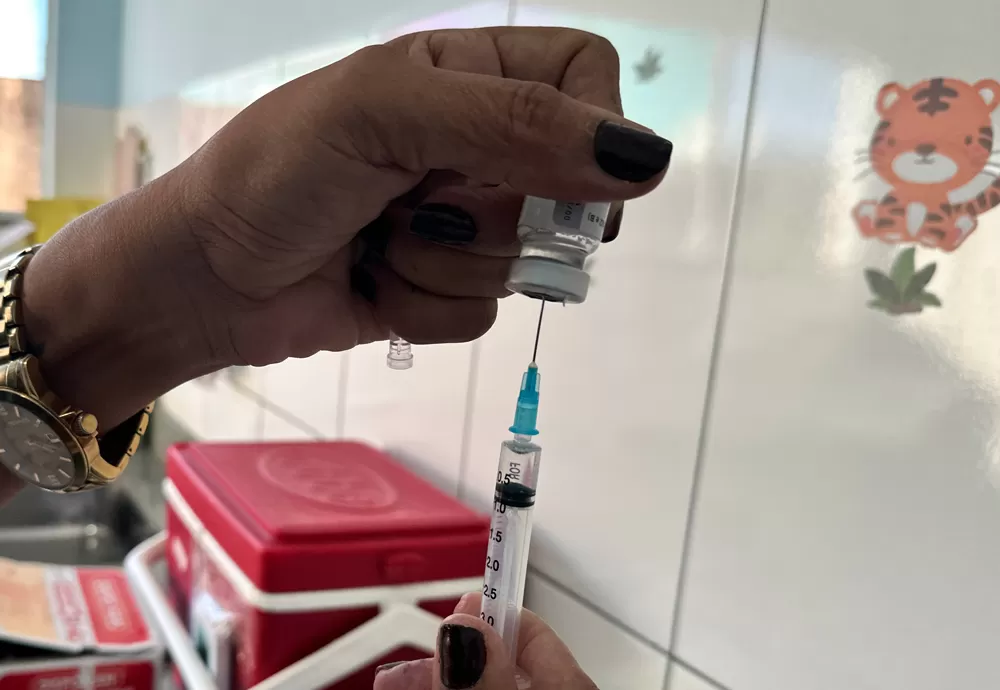
Aprovada pela Agência Nacional de Vigilância Sanitária (Anvisa) no início de dezembro, a Butantan-DV é o primeiro imunizante contra a dengue em dose única no mundo. A vacina foi testada para ser aplicada em pessoas com idade de 12 a 59 anos.
Em cerimônia na capital paulista, o ministro da Saúde, Alexandre Padilha, destacou que a imunização abrange todas as equipes multiprofissionais de unidades básicas de saúde, incluindo agentes comunitários, enfermeiros, médicos e demais profissionais cadastrados.
O ministro e o presidente da República, Luiz Inácio Lula da Silva, também visitaram nesta manhã o Centro de Produção de Vacina contra a Dengue (PVD) do Instituto Butantan, em São Paulo.
“Um dia histórico. Não tenho dúvida nenhuma de que, hoje, nós estamos presenciando um marco histórico que vai colocar o Butantan entre os maiores complexos de inovação tecnológica e industrial do mundo”, disse Padilha.

A vacina contra a dengue produzida pelo Instituto Butantan pode ser aprovada a partir do final da semana que vem pela Agência Nacional de Vigilância Sanitária (Anvisa). O anúncio foi feito nesta sexta (7), em coletiva de imprensa que tratou sobre a necessidade de acelerar as filas para aprovação de medicamentos sintéticos e produtos biológicos.
“A vacina de dengue do Butantan é um processo prioritário para a agência”, afirmou o diretor da Anvisa Daniel Pereira. Ele explicou que, na semana passada, houve uma reunião com o comitê de especialistas para suprir dúvidas que ficaram em relação à vacina.
“A nossa expectativa é que, na primeira quinzena de novembro ainda, ou alguns dias a mais, a gente já tenha uma conclusão por parte da Anvisa, para a gente autorizar o registro”, explicou.
Pereira acrescentou que essa análise demandou “muitas horas” de discussão técnica com especialistas externos que apoiaram a decisão. Segundo a Anvisa, não houve solicitações de registro de outros imunizantes por parte dos demais laboratórios.
O Instituto Butantan, órgão ligado à Secretaria do Estado da Saúde de São Paulo, recebeu nesta terça (1º) a aprovação da Agência Nacional de Vigilância Sanitária (Anvisa) para o início dos ensaios em humanos, da sua candidatura à vacina contra a gripe aviária A (H5N8). Para isso, o Instituto pretende recrutar 700 adultos e idosos voluntários que participarão das fases 1/2 do estudo em cinco centros de pesquisa brasileiros. A vacina influenza monovalente A (H5N8) (inativada, fragmentada e adjuvada) será testada em duas doses com intervalo de 21 dias, primeiramente em adultos de 18 anos até 59 anos e 11 meses e depois em pessoas com 60 ou mais. O Instituto Butantan concluiu os estudos pré-clínicos com resultados específicos de segurança e imunogenicidade. "Estamos em conversas com o Ministério da Saúde, que se mostrou sensível ao avanço dessa discussão. Com a plataforma aprovada, o Instituto pode produzir um contingente de 30 milhões de doses após os resultados iniciais. Este contingente estratégico pode ser utilizado caso o vírus comece a se disseminar entre humanos e tenha esperanças semelhantes às representadas pela vacina candidata do Instituto Butantan", afirma o diretor do Instituto Butantan, Esper Kallás. O Ministério da Saúde publicou em dezembro de 2024 um Plano de Contingência Nacional do Setor Saúde para Influenza Aviária no qual define as estratégias que devem adotar em caso de situação de emergência relacionada à doença. Uma delas é provar estoques estratégicos de medicamentos e insumos que podem combater a disseminação da doença.